Betaína en alimentación de rumiantes
F.J. Giráldez1, M. Dehnavi1, S. Bettini2, A. Díaz1, C. Ruano3, A. Antolin4, A.B. Rodriguez5, J. Amor5, S. Andrés1
1 Instituto de Ganadería de Montaña. Consejo Superior de Investigaciones Científica. Universidad de León. Grulleros, León. España
2 Dpto. Agricultura, Alimentación y Ciencias Ambientales. Universidad Perugia. Italia
3 KWS Semillas Ibérica SLU. Zaratán, Valladolid. España.
4 Timac Agro. Orkoyen, Navarra. España
5 Industrias de Nutrición Animal, SL (INATEGA). León. España
La betaína, conocida también como trimetil-glicina, es un compuesto con múltiples funciones, que se lleva utilizando en alimentación animal desde hace varias décadas. Inicialmente, el interés de su empleo residía en su efecto lipotrópico y osmoprotector, que lo convertían en un compuesto útil para modificar la composición de la canal e incrementar la resistencia al estrés, causado fundamentalmente por calor. En alimentación animal, su empleo se ha centrado mayoritariamente en especies no rumiantes, si bien su uso es cada vez más frecuente en rumiantes, especialmente en vacuno de leche, en etapas críticas, como el periodo perinatal.
No obstante, estudios recientes señalan un papel más diverso y complejo de la betaína, interviniendo en la fisiología digestiva y salud intestinal y en la regulación del sistema inmunitario, pero también en el desarrollo cognitivo y en la programación metabólica de la descendencia, lo que aporta una nueva dimensión a su empleo. En este artículo se revisarán los mecanismos biológicos implicados y su empleo en diferentes etapas productivas, en las especies rumiantes.
Fuentes de betaína
La betaína presente en los tejidos de los animales puede ser de origen exógeno, es decir, aportada por la dieta, o endógeno, sintetizada en el propio organismo.
La betaína se encuentra en concentraciones significativas en algunos vegetales, como la remolacha o el trigo y subproductos relacionados, como las melazas o el salvado (Eklund et al., 2005; Dobrijevic et al., 2023). De hecho, el nombre de betaína se debe a que se aisló por primera vez en jugo de la remolacha azucarera (Beta vulgaris). Consumos diarios de hasta 50 g/animal en vacuno y 6 g en ovino y caprino adulto se consideran seguros y son difícilmente alcanzables con las dietas estándar usadas en estas especies, independientemente del nivel productivo. A modo de ejemplo, una oveja adulta debería consumir 1,7 kg de melaza concentrada de remolacha o 4,3 kg de salvado de trigo para alcanzar un consumo de 6 g de betaína al día. Se puede estimar que el consumo de una oveja en lactación, consumiendo 2,8 kg de materia seca de una ración que incluya salvado de trigo y melaza de remolacha (materias primas con elevado contenido de betaína), podría situarse alrededor de 1,5 g de betaína/animal y día (ver figura 1). En general, el contenido de betaína en las raciones de rumiantes se considera traza (Mitchell et al., 1979).
Como se analiza con mayor detalle en apartados posteriores, diferentes estudios señalan que el efecto de la betaína es dosis dependiente y se requieren concentraciones superiores para potenciar los efectos beneficiosos. Por ello, la betaína se comercializa también como aditivo alimentario, pudiendo incluirse tanto en el pienso como en el agua de bebida, ya que es soluble en agua. Es un compuesto termoestable por lo que no se destruye en cantidades significativas durante la fabricación del pienso. Como aditivo se comercializa, fundamentalmente, en forma de clorhidrato de betaína (C5H12ClNO2) o betaína anhidra (C5H11NO2). La primera incluye en la molécula un átomo de cloro, por lo que el porcentaje de betaína es de alrededor del 76% y tiene un balance electrolítico negativo. La betaína anhidra es neutra desde el punto de vista del balance electrolítico y la riqueza es superior al 98%. En rumiantes, la betaína puede ser parcialmente degradada en el rumen y, por ello, se han desarrollado aditivos que la protegen de la degradación, incrementado su absorción en el intestino.
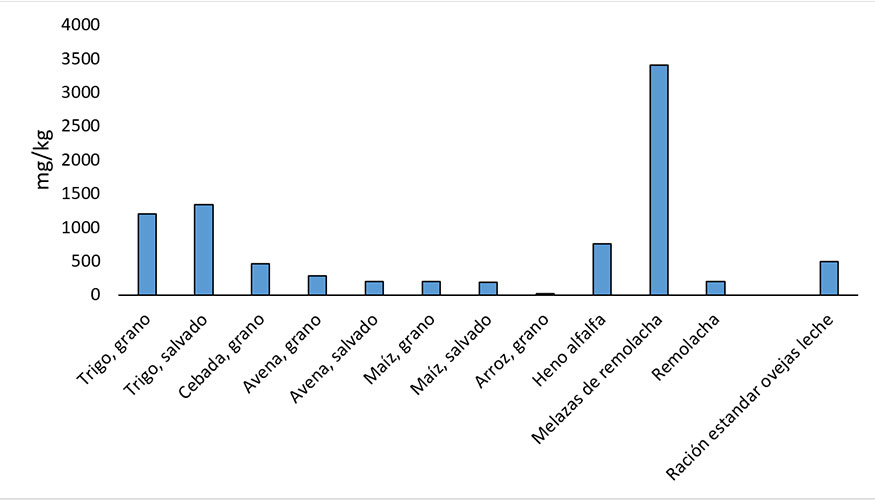
Figura 1. Contenido de betaína en diferentes alimentos de uso ganadero y en una ración comercial empleada en ovino de leche.
Ración comercial ovejas de leche: 37% heno de alfalfa, 6% paja de cebada, 2% de salvado de trigo, 11% cascarilla de soja, 7,5% cebada, 14,5% de maíz, 12% torta de soja, 4% de melaza de remolacha, 1,5 grasa protegida, 0,5% urea, 2% bicarbonato de sodio y 1,7% de corrector vitamínico-mineral.
Absorción y síntesis de betaína
En general, la digestibilidad de la betaína es mayor cuando se administra en forma purificada, que cuando es incorporada de forma natural a través de los alimentos (Kettunen et al., 2001). En los rumiantes, la betaína puede ser utilizada por la microbiota, pero diferentes estudios, tanto in vitro como in vivo, señalan que una proporción significativa escapa a la degradación ruminal (Loest et al., 2000; Nakai et al., 2013).
La betaína aportada por la dieta se absorbe a nivel intestinal, a través de dos sistemas específicos de transporte activo: sistema de transporte Na dependiente de aminoácidos (tipo A) y sistema Na independiente BGT-1 (Betaína-Gamma aminobutírico) (Craig, 2004). Tras pasar a los enterocitos se difunde al torrente sanguíneo, incrementándose temporalmente la concentración plasmática. En la especie humana se ha observado que, tras la administración puntual en una única dosis, la concentración en sangre aumenta rápidamente, alcanzándose un pico máximo de concentración alrededor de las 2 horas, tras el cual decrece, presentando a las 24 horas valores similares a los registrados antes de la administración del suplemento (Craig, 2004; Atkinson et al., 2008). En un estudio realizado en ovejas gestantes (Brougham et al., 2020), que consumieron 2 ó 4 g/día de betaína, con la ración, se observó también una variación en la concentración plasmática a lo largo del día, alcanzándose un pico tras 8 horas de recibir el pienso con betaína. En general, la respuesta es dosis dependiente, de forma que a mayor ingestión de betaína, mayor es la concentración plasmática en el pico máximo. No obstante, la administración continua de betaína permite incrementar su concentración en diferentes tejidos y órganos, fundamentalmente en intestino, hígado o riñón, pero también en tejido muscular o adiposo (Kettunen et al., 2001; Slow et al., 2009).
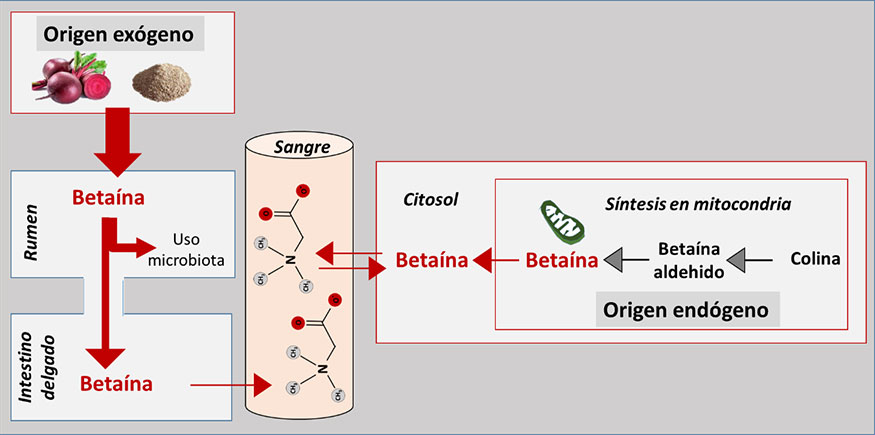
La betaína puede ser también de origen endógeno, siendo sintetizada a partir de la colina. La síntesis se produce, fundamentalmente, en la mitocondria de los hepatocitos, aunque también en otros órganos y tejidos, mediante la acción de las enzimas colina oxidasa – que transforma la colina en betaína aldehído – y la betaína aldehído deshidrogenasa, que transforma la betaína aldehído en betaína (ver figura 2). La betaína no puede ser metabolizada dentro de la mitocondria y por ello, una vez sintetizada, difunde hacia el citosol y, a través del torrente sanguíneo, puede difundirse a otros tejidos. Cabe señalar que la betaína puede ser excretada desde el hígado, a través de la bilis, al intestino (circuito enterohepático), donde puede ser utilizada por la microbiota o ser reabsorbida.
Las bacterias pueden sintetizar betaína a partir de colina y de la carnitina, pero algunas especies halófilas y halotolerantes pueden sintetizar betaína a partir de glicina, a través de reacciones de metilación (Nyyssölä et al., 2000; Meadows & Wargo, 2015; Liu et al., 2022). Se han identificado bacterias halotolerantes en el rumen (Chantarasiri, 2014), pero se desconoce la importancia cuantitativa de la síntesis de betaína en la microbiota ruminal y su contribución a la betaína que llega al intestino.
Funciones esenciales de la betaína
La betaína puede desarrollar diferentes funciones, siendo la osmoprotección, la donación de grupos metilo y la modulación de la composición y actividad de la microbiota del tracto digestivo, las más relevantes. A través de estas funciones puede desarrollar diferentes efectos en la fisiología digestiva y en el metabolismo y, como consecuencia, en la competencia inmunitaria y en el rendimiento productivo y reproductivo de los animales.
Osmoprotección. Tanto las células vegetales, como las animales y las bacterias acumulan sustancias que contribuyen a regular la presión osmótica, manteniendo la estructura y función de las proteínas y la integridad celular en situaciones de estrés. Estas sustancias se conocen como osmolitos y se clasifican en dos grandes grupos: compatibles, como la betaína, el inositol, la urea o el sorbitol, que permiten adaptarse a las células sin causar daño, e incompatibles, que son aquellos que en elevadas concentraciones alteran las estructura y función de las proteínas (Dobrijevic et al., 2023), causando daño celular. En este último grupo se encuadraría por ejemplo los iones inorgánicos (sodio, potasio, cloro).
En situaciones de estrés osmótico, causado por déficit hídrico o consumo de agua salina, las células usan, inicialmente, electrolitos como el sodio o el potasio para mantener el balance hídrico y la integridad celular, pero este mecanismo es costoso energéticamente y la acumulación intracelular de iones desestabiliza las estructuras proteicas, se produce estrés oxidativo y daño en el ADN. En esta situación, se detiene el ciclo celular, proporcionando tiempo y recursos para adaptarse.
Uno de los mecanismos de adaptación es la acumulación de osmolitos orgánicos, como la betaína, que es el osmolito más ampliamente distribuido en la naturaleza. Mediante la acumulación de osmolitos y el incremento en la expresión de genes codificadores de proteínas protectoras, como las proteínas de choque térmico (chaperonas), se normaliza el volumen celular y la fuerza iónica y se estabilizan las proteínas, recuperándose la actividad celular. En el caso concreto de la betaína, el incremento en la concentración no parece producirse por un aumento en la síntesis endógena, sino por una mayor disponibilidad del transportador BGT-1, tanto por un incremento en la síntesis, como en una migración desde el citosol a la membrana (Burg et al., 2006). A través de estas modificaciones, se produce un trasvase de betaína desde la sangre al interior de la célula. La betaína además de regular la presión osmótica, modula también la capacidad antioxidante y la respuesta inflamatoria y aumenta la expresión de la proteína antiapoptótica Bcl-2, reduciendo el daño asociado al incremento en la presión osmótica (Xu et al., 2021).
Donación de grupos metilo. La betaína ejerce funciones similares a la metionina y colina, actuando como un compuesto donador de grupos metilo. Como refleja la figura 3, la betaína dona un grupo metilo a la homocisteina, transformándose la primera en dimetilglicina y la segunda en metionina. La remetilización de la homocisteina es principalmente dependiente de la betaína en el hígado y riñón, siendo más importante la remetilación dependiente del ciclo del folato en el resto de tejidos.
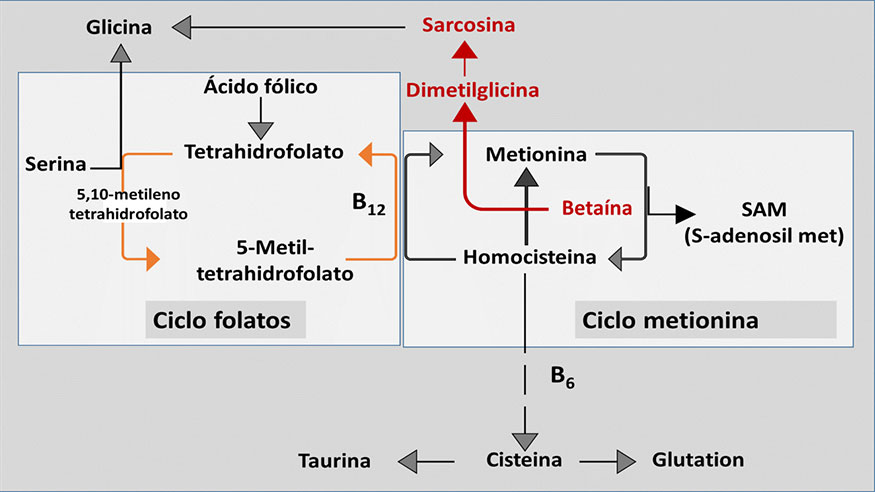
La dimetilglicina puede donar un nuevo grupo metilo, transformándose en sarcosina, la cual puede volver a ceder otro grupo metilo, transformándose en glicina. En los mamíferos no es posible la síntesis de betaína a partir de glicina, por lo que ésta se incorpora al pool de aminoácidos, cumpliendo diferentes funciones. La eficiencia de metilación de la betaína es similar a la de la metionina, pero superior a la de la colina.
A través de la donación de grupos metilo y la síntesis de metionina y de S-adenosil metionina, la betaína interviene en la regulación de la replicación celular, la expresión génica y en múltiples rutas metabólicas, modulando el metabolismo proteico, lipídico y glucídico, la capacidad antioxidante y la respuesta inmunitaria. Para más información relacionada con la metionina y el papel de la metilación se puede consultar un artículo publicado por nuestro grupo (Andrés et al., 2025).
Chaperona química. Las proteínas están desplegadas cuando se sintetizan de novo y deben adquirir su conformación tridimensional para realizar sus funciones biológicas. Las proteínas pueden desplegarse para atravesar las membranas de ciertos orgánulos celulares o cuando son desnaturalizadas por diferentes fuentes de estrés (p.ej., estrés salino o térmico) (Dave & Gruebele, 2015). Cuando las proteínas están desplegadas se pueden plegar incorrectamente o entrelazarse entre ellas formando agregados aberrantes, lo que puede causar diferentes patologías (Balchin et al., 2016). La formación de estructura amiloides podría citarse como un ejemplo de las consecuencias negativas de una agregación perjudicial de proteínas (Buchner, 2019).
Las células disponen de sistemas de protección, como son las chaperonas, que son las responsables de que las proteínas se plieguen correctamente y de conferir estabilidad a su estructura en condiciones fisiológicas normales. No obstante, la expresión de algunas chaperonas se incrementa en situaciones de estrés que causan cambios conformacionales en las proteínas. En este sentido, una de las chaperonas más conocidas son las denominadas proteínas de choque térmico (HSP), que incluye varias familias (HSP40, HSP60, HSP70, HSP90 y HSP110) (Nava & Hansberg, 2020).
No obstante, en la célula existen otros compuestos – que no son proteínas - que pueden actuar como chaperonas, y que se dividen en dos grandes grupos: osmolitos y compuestos hidrofóbicos. Entre las primeras se pueden citar la betaína o la oxido-trimetil amina (TMAO) y entre los compuestos hidrofóbicos algunos derivados de los ácidos biliares, como los ácidos ursodeoxicólico y tauroursodeoxicólico (Diamant et al., 2001; Kusaczuk, 2019). Los mecanismos de acción parecen ser tanto directos – interaccionando con las proteínas – como indirectos, regulando la expresión de las chaperonas proteicas, si bien el mecanismo no está completamente esclarecido y podría variar entre compuestos. Incluso algunos osmolitos pueden actuar como estabilizantes o desestabilizantes de la estructura proteica dependiendo de su concentración y del tipo de proteína (Ortiz-Costa et al., 2002).
Efecto de la betaína en la utilización digestiva
Diferentes estudios señalan que la administración de betaína mejora la utilización digestiva. Así, por ejemplo, se ha señalado que se incrementa la digestibilidad de la grasa, lo que se ha asociado con un efecto estimulante de la secreción biliar y de la síntesis de quilomicrones, implicados en la absorción de la grasa (Eklund et al., 2005; Wang et al., 2020). A modo de ejemplo, en algunas patologías, como la abetalipoproteinemia o síndrome de Bassen-Kornzweig, se produce un déficit en la síntesis de quilomicrones en los enterocitos, que reduce el transporte de lípidos desde el intestino al hígado, causando una malabsorción de la grasa e hipolipidemia (Argueso-Argüeso et al., 2011).
Cuando los animales consumen dietas con elevado contenido de grasa saturada se incrementa la síntesis de colesterol (Nestel et al., 1978). En estas condiciones, la administración de betaína puede incrementar la actividad de las enzimas HMGCR, que interviene en la síntesis de colesterol, y CPT1, que favorece la oxidación de los ácidos grasos, generando acetil-CoA, que es el principal sustrato a partir del cual se sintetiza el colesterol (Li et al., 2020). No obstante, la betaína puede también incrementar la actividad de la enzima colesterol 7α-hidrolasa, que interviene en la ruta de síntesis de ácidos biliares a partir del colesterol, y de la bomba transportadora de sales biliares, lo que aumenta la secreción biliar hacia el intestino, favoreciendo la digestión de la grasa (Li et al., 2020). En estas condiciones, la betaína no reduce el colesterol en sangre, ya que la eliminación a través de la síntesis de ácidos biliares, se compensa por el incremento en la síntesis de colesterol. Sin embargo, en dietas con bajo contenido de grasa, la betaína puede ejercer un efecto hipocolesterolémico, aunque es un efecto que parece depender de la dosis de betaína y puede causar un incremento de la concentración de colesterol-LDL (Olthof et al., 2005). Este efecto de la betaína sobre la concentración de LDL se ha asociado con un incremento en la disponibilidad de colina para la síntesis de fosfatidilcolina, que forma parte de las lipoproteinas de muy baja densidad (VLDL), precursoras del LDL (Olthof et al., 2005). No obstante, cuando hay carencia de fosfatidilcolina, el colesterol y los triglicéridos se acumulan dentro del citosol de los hepatocitos, lo que favorece la aparición de hígado graso (Zeisel, 2006).
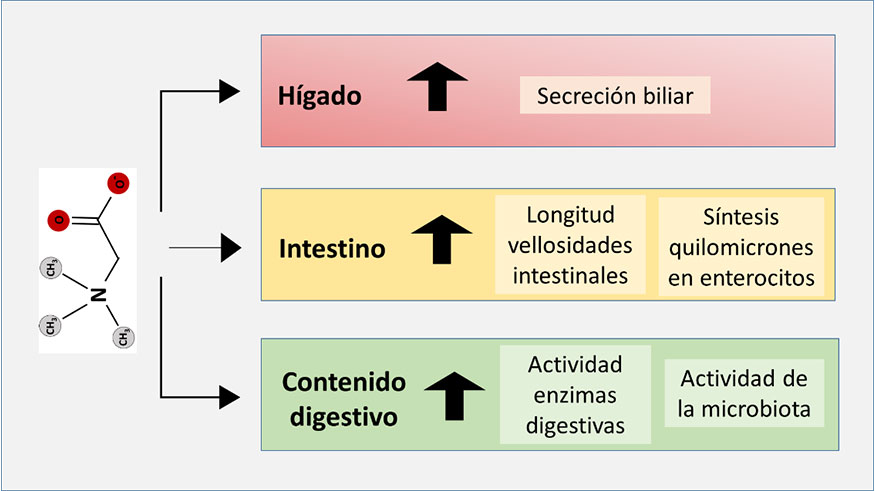
Estudios en especies monogástricas señalan un incremento en la actividad de diferentes enzimas (amilasa, lipasa, tripsina, quimotripsina) en el duodeno y en la digestibilidad de la materia orgánica, proteína y grasa (Wang et al., 2020). Este efecto sobre la actividad enzimática es incluso mayor cuando los animales sufren estrés osmótico (Wang et al., 2018) y parece estar relacionado con una optimización de la interfaz agua-proteína, que favorece la actividad catalítica.
El efecto positivo sobre la utilización digestiva también podría estar relacionado con la morfología intestinal. En este sentido, en diferentes especies (ratones, aves, cerdos y conejos) se ha observado que la administración de betaína incrementa la longitud de las vellosidades intestinales y la profundidad de las criptas (Wang et al., 2018, 2020; Liu et al., 2019; Li et al., 2024). Además, su papel como osmolito protege a las células intestinales de las variaciones en la presión osmótica, consustanciales con las variaciones en la ingestión de alimento y de agua (Perumal et al., 2025).
En rumiantes, en condiciones fisiológicas normales, se ha observado un incremento en la actividad de la microbiota, incrementándose la producción de ácidos grasos volátiles y un cambio en el patrón, incrementándose la proporción de acetato y butirato y disminuyendo la concentración de propionato (Shah et al., 2020; Liu et al., 2021; Ghoneem & El-Tanamy, 2023). Estos cambios en la fermentación ruminal están asociados a un incremento en la población bacteriana y en la actividad de las enzimas microbianas (celulasa, celobiasa, xilanasa, pectinasa, amilasa y proteasa), que se traducen en un incremento de la digestibilidad de la proteína y de los carbohidratos estructurales (Liu et al., 2021). En especies no rumiantes también se ha observado una modificación de la composición de la microbiota en el intestino grueso y un incremento en la producción de ácidos grasos volátiles y ácido láctico en el intestino (Wang et al., 2020, 2025).
La betaína puede ser catabolizada por la microbiota del tracto gastrointestinal, generando trimetil amina (TMA) (Mahmood et al., 2020). La TMA se puede absorber en el intestino, pero, en el caso de los rumiantes, puede ser utilizada por algunas especies de arqueas (Thermoplasmata spp) para producir metano (via metilotrófica), como ruta alternativa a la hidrogenotrófica, en la que se utiliza CO2 e H2 como precursores (Mitchell et al., 1979; Poulsen et al., 2013). No obstante, no hay evidencias consistentes que indiquen que la administración de betaína en rumiantes incremente la producción de metano de forma significativa.
Efecto de la betaína en el metabolismo
La betaína regula expresión de genes relacionados con el metabolismo de los lípidos y carbohidratos, fundamentalmente a través de su papel como donador de grupos metilo.
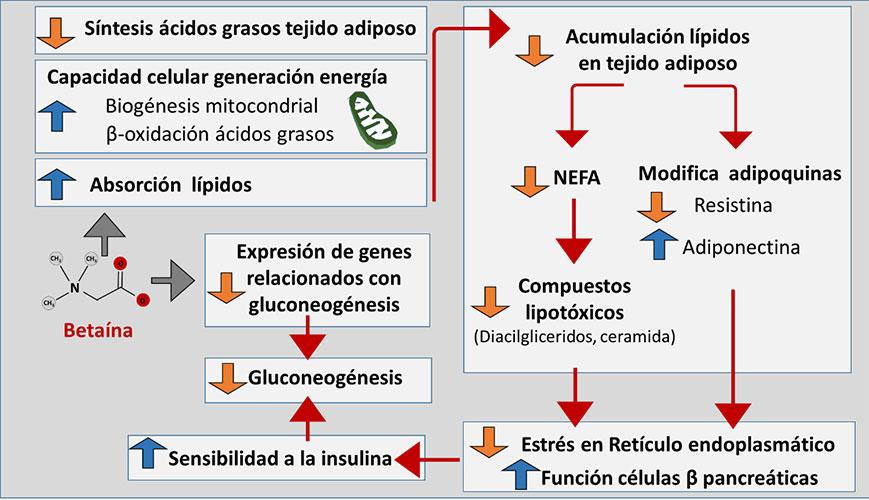
En relación con el metabolismo lipídico, la betaína modula la absorción de lípidos en el intestino, promueve la oxidación de ácidos grasos e inhibe la lipogénesis (ver figura 5). La betaína inhibe la expresión de múltiples genes relacionados con la síntesis de AG y estimula la expresión de PGC1α (coactivador 1 alfa del receptor activado por proliferador de peroxisomas gamma), ACOX1 (Acil-CoA oxidasa 1) y CPT1 (carnitina palmitoil transferasa), implicados en la biogénesis mitocondrial y la oxidación de AG, así como de diferentes proteínas (MTTP y ApoB) involucradas en la síntesis de lipoproteína de muy baja densidad (VLDL) (Zhang et al., 2019; Fan et al., 2022). Estos efectos parecen estar mediados por una supresión de la expresión de ARN codificante de metilasas y un incremento en la expresión de ARN codificante de demetilasas. En este sentido, se ha observado que cuando se utilizan células mutantes con actividad demetilasa se bloquea el efecto de la betaína (Zhang et al., 2019).
El efecto de la betaína sobre el metabolismo glucídico está interconectado con el metabolismo lipídico. En general, la acumulación excesiva de tejido adiposo está asociada con un incremento en la concentración en plasma y en los tejidos de ácidos grasos no esterificados (NEFA), a partir de los cuales se puede generar compuestos lipotóxicos (p.ej., diacilglicéridos o ceramidas) que causan daño celular, como estrés en el retículo endoplasmático y disfunción mitocondrial (Szkudelska & Szkudelski, 2022).
Efecto de la betaína en la respuesta inmunitaria e integridad intestinal
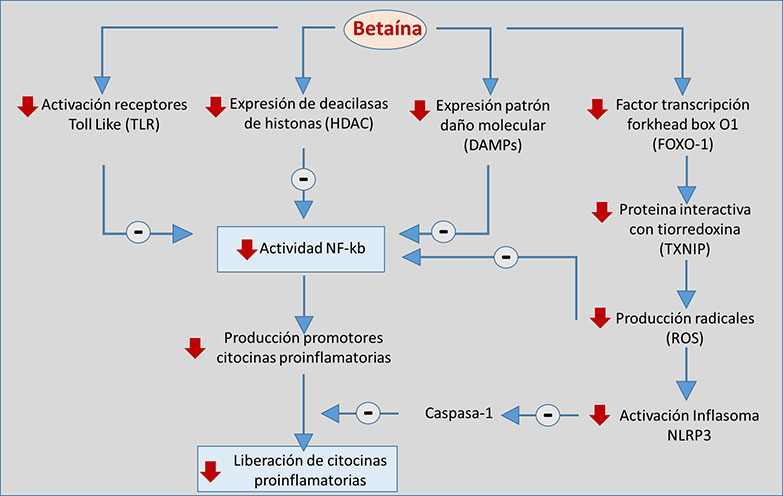
No se conoce con precisión las bases moleculares del efecto de la betaína sobre la respuesta inflamatoria. Diferentes estudios señalan que la betaína podría inhibir la ruta de señalización asociada al factor nuclear (NF-kB) y la activación del inflasoma NLRP3. A través de este mecanismo se reduciría la producción de precursores de citoquinas proinflamatorias y su posterior maduración y liberación (ver figura 6).
La inhibición de la activición de NF-Kb se ha asociado con una inhibición de receptores TLR, una reducción en la expresión de deacilasas de histonas - que regularían la expresión génica- y en una modificación en el patrón molecular asociado al daño (DAMPs), que son moléculas que se unen a receptores tipo Toll en las células inmunitarias, desencadenando una cascada de señalización que conduce a la liberación de citoquinas proinflamatorias (Zhao et al., 2018; Shi et al., 2019). No obstante, se ha observado también que la administración de betaína inhibe el factor de transcripción forkhead Box-1, que reduce la producción de radicales oxidativos, inhibiendo la activación del inflasoma NLRP3, implicado en el procesado y liberación de las citoquinas (Zhao et al., 2018).
Utilización de betaína en diferentes estados productivos (gestación, cebo y lactación)
Empleo en gestación. Se ha observado que la administración de betaína en animales gestantes modifica la metilación y la expresión de genes relacionados con la gluconeogénesis y el metabolismo del colesterol en la descendencia, pero sin un efecto consistente en el peso al nacimiento, en la tasa de supervivencia o en la ganancia de peso durante la lactancia (Cai et al., 2014; 2016; Brougham et al., 2020; 2024). Así, por ejemplo, en ovejas gestando dos corderos, la administración de 4 g/día de betaína durante la segunda mitad de la gestación redujo el tiempo entre el nacimiento y el primer amamantamiento y la mortalidad en la primera semana de vida, pero no influyó en el peso al nacimiento ni en el peso destete (Brougham et al., 2020). Sin embargo, en ovejas con gestación simple, la suplementación de 4 g/día de betaína desde el día 125 de gestación incrementó el peso al destete, pero no influyó en el peso al nacimiento ni en la tasa de supervivencia (Brougham et al., 2024). Con aportes de betaína inferiores (2 g/día), durante toda la gestación o durante el último mes, no se observaron efectos positivos en la tasa de supervivencia, ni resultados concluyentes sobre el peso al destete (Brougham et al., 2020; 2024). Sin embargo, se ha señalado que aportes superiores (5 g/día), durante el último mes de gestación y en condiciones de estrés térmico, incrementan el peso al nacimiento de los corderos, pero sin efecto en la ganancia diaria de peso durante la lactancia (Sahraei et al., 2020; Yarahmadi et al., 2020). En un estudio reciente, realizado por nuestro grupo de investigación (Giráldez et al., 2025), financiado por el proyecto PID2021-126489OB-I00, se observó que el consumo de alrededor de 5 g/día, en ovejas durante el último tercio de la gestación, redujo la ingestión de alimento, tanto en la etapa de gestación, como durante el primer mes de lactación, pero no influyó en el peso de los corderos al nacimiento, en la tasa de supervivencia en la primera semana, ni en la ganancia de peso durante la lactancia (ver figura 7). El tipo de parto (simple vs múltiple) tampoco modificó el efecto de la betaína sobre el peso al nacimiento.
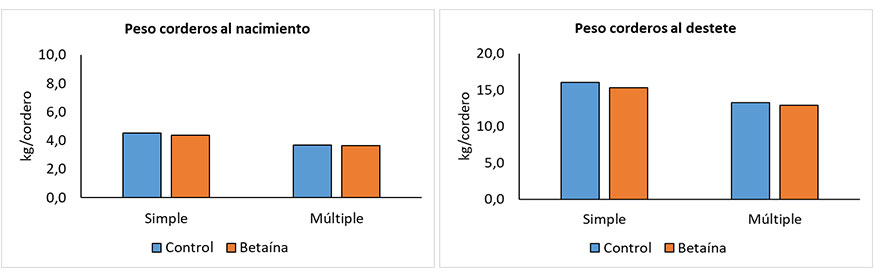
Figura 7. Efecto de la administración de betaína durante el último tercio de gestación en ovejas de parto simple y múltiple sobre el peso vivo al nacimiento y al destete.
Resultados del proyecto PID2021-126489OB-I00. Las ovejas fueron alimentadas ad libitum con una dieta mixta completa granulada, incluyendo en la dieta del grupo betaína 4 g/kg del aditivo. La lactancia tuvo una duración de 38 días.
Los resultados obtenidos hasta la fecha permiten concluir que la administración de betaína en rumiantes en gestación no es perjudicial, pero no siempre ejerce un efecto beneficioso. La ausencia de resultados concluyentes podría deberse a que el efecto parece variar con la dosis administrada, con el momento y duración de la suplementación, el tipo de gestación o las condiciones ambientales, por lo que es necesario realizar nuevos estudios que permitan establecer las condiciones en las que podría ser beneficioso la suplementación con betaína. Tampoco debe descartarse el tipo de dieta, ya que dependiendo de los ingredientes podría variar el aporte no solo de betaína, sino de compuestos relacionados con su metabolismo, como la colina o la metionina.
Empleo en lactación. Diferentes metaanálisis señalan que la administración de betaína en vacas de leche incrementa la ingestión de materia seca y la producción de leche, tanto en situaciones de termoneutralidad como de estrés por calor (Abhijith et al., 2024; Malik et al., 2024). En la especie ovina y caprina se han realizado menos estudios, pero apuntan también a un incremento en la producción de leche (Fernandez et al., 2004; Abhijith et al., 2024).
En vacas en la lactación temprana (primeras 8 semanas), se ha observado que la suplementación con betaína incrementa la producción de leche y la ingestión, si bien el incremento de ingestión no es suficiente y se incrementa el balance energético negativo (Monteiro et al., 2016). En estas condiciones los animales movilizan sus reservas lipídicas y se corre el riesgo de que se produzca esteatosis hepática (acumulación de grasa en hígado) si se supera la capacidad de oxidación de los ácidos grasos y se limita su transporte hacia otros tejidos.
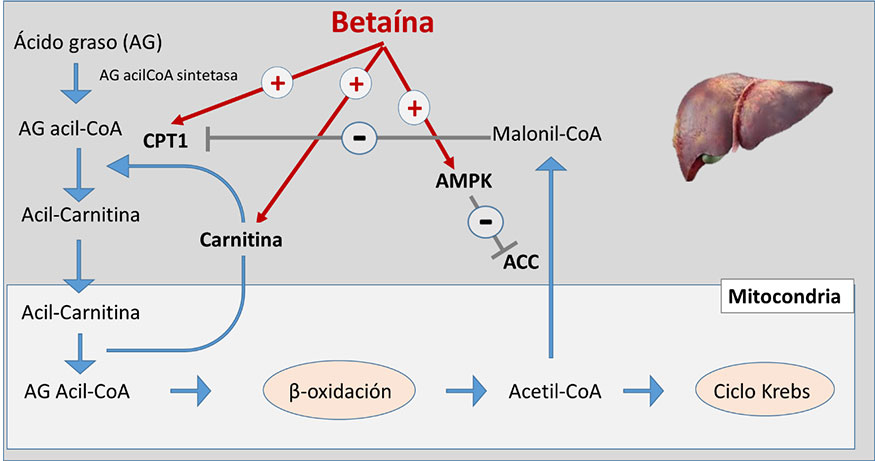
Figura 8. Mecanismo a través del cual la betaína estimula la β-oxidación de los ácidos grasos en el hígado.
CPT1: carnitina palmitoil transferasa; ACC: Acetil-CoA carboxilasa; AMPK: proteína quinasa actividad por AMP.
La betaína puede influir en ambos procesos, ya que, por una parte, estimula la β-oxidación (ver figura 8), incrementando la expresión de la enzima carnitina palmitoil transferasa (CPT1), que transfiere la carnitina a los ácidos grasos de cadena larga, permitiendo que atraviesen la membrana mitocondrial y puedan ser oxidados. En relación con la β-oxidación, la betaína también puede estimular la síntesis de carnitina y activar la ruta de la proteína quinasa activada por AMP (AMPK), inhibiendo la actividad de la acetil-coA carboxilasa (ACC) y como consecuencia la síntesis de malonil-Coa, que es un inhibidor alostérico de la enzima CTP1 (Zhao et al., 2018).
Por otra parte, el hígado elimina el exceso de triglicéridos, transportándolos a otros tejidos, a través de la síntesis de lipoproteínas de muy baja densidad (VLDL), que son liberadas al torrente sanguíneo, interaccionando con otras lipoproteínas y tejidos y transformándose en otras lipoproteínas (VLDL maduras, VLDL remanentes, LDL intermedias y LDL) (ver figura 9). La síntesis de VLDL se realiza ensamblando los triglicéridos y el colesterol con fosfolípidos y la apolipoproteinas (Apo B-100, C-II, C-III, E y A5) (Chen et al., 2024). Los fosfolípidos se disponen en una monocapa en la superficie y gracias a su carácter anfipático permiten a las VLDL dispersarse y ser transportadas en el plasma. La fosfatidilcolina es el componente principal y se sintetiza a partir de la colina, de manera que una deficiencia de colina reduce la capacidad de síntesis hepática de VLDL, favoreciendo la aparición de hígado graso (Yao & Vance, 1988; Arshad et al., 2024). La administración de betaína puede reducir las necesidades de colina para la donación de grupos metilo, por lo que aumenta la disponibilidad de colina para otras funciones, como la síntesis de fosfatidilcolina.
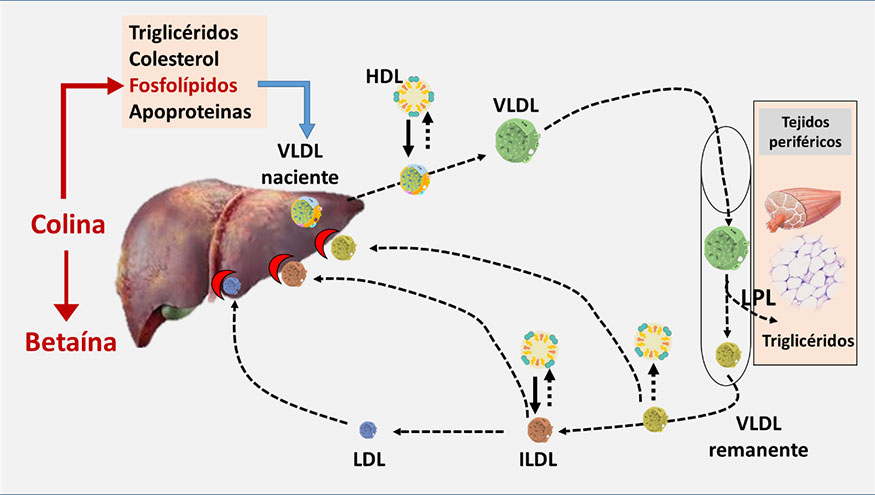
Figura 9. Transporte de triglicéridos desde el hígado a otros tejidos y relación con la colina y la betaína.
LPL: Lipoprotein lipasa; HDL, VLDL, ILDL, LDL: lipoproteínas de densidad alta, muy baja, intermedia y baja.
En relación con el efecto de la betaína sobre la composición química de la leche los estudios realizados no arrojan resultados concluyentes. Algunos estudios señalan un incremento en el contenido de grasa, si bien el mecanismo no está completamente esclarecido. En este sentido, se apunta, por una parte, a un incremento en la disponibilidad de ácidos grasos preformados disponibles para la glándula mamaria, asociados al efecto lipotrópico de la betaína (Monteiro et al., 2016). No obstante, este efecto se ha asociado también con el hecho de que la betaína en el rumen puede incrementar la producción de ácido acético, que es un precursor de los ácidos grasos de cadena corta que se secretan en la leche (Fernandez et al., 2004).
Empleo en crecimiento-cebo. Diferentes estudios sugieren que la administración de betaína puede mejorar la ingestion, la ganancia diaria de peso y el índice de conversion en vacuno y ovino, disminuyendo, además, la deposición de grasa corporal (Abdelsattar et al., 2019; Dong et al., 2020; Abhijith et al., 2024). Cabe señalar, no obstante, que estos efectos no siempre se observan (Abdelsattar et al., 2019; Jin et al., 2021; Buonaiuto et al., 2025) e incluso algunos estudios señalan efectos negativos sobre la ingestión, en la ganancia diaria de peso o el indice de conversion (López et al., 1997; Abdelsattar et al., 2019).
Conclusiones
Los efectos positivos de la suplementación con betaína en rumiantes, en los diferentes estados fisiológicos, estarían relacionados con los efectos descritos sobre la microbiota, la utilizacion digestiva y el metabolismo lipídico, así como sobre la integridad intestinal, el estatus antioxidante y el sistema inmunitario. Estos efectos beneficiosos se observan en mayor medida en situaciones estresantes para los animales, ya sean de naturaleza metabólica (p.ej., vacas en transición), infecciosa o ambiental (p.ej., estrés por calor o hídrico).
La betaína, por tanto, tiene potencial para ser considerado un aditivo eficaz en rumiantes, si bien es necesario continuar los trabajos de investigación para identificar los factores que modulan su efecto y establecer - sobre bases científico-técnicas - recomendaciones que permitan un uso eficiente, rentable y seguro.
Referencias bibliográficas
En poder de los autores a disposición de los lectores interesados.
Oviespaña, noticias diarias sobre el mercado nacional e internacional del ovino, investigación ganadera, alimentación y sistemas de manejo.





