El diagnóstico laboratorial: Una herramienta indispensable para el control de las diarreas

SEGUNDA SESIÓN / Seminario Exopol. Diagnostico de diarreas en corderos Lactantes.
CELIA SANZ TEJERO. Responsable de Microbiología en EXOPOL.
Se define como diarrea la alteración intestinal que se caracteriza por la mayor frecuencia, fluidez y, a menudo, volumen de las deposiciones. Sin embargo, la diarrea no es propiamente una enfermedad como tal, sino un síndrome producido por multitud de factores que se caracteriza además por producir deshidratación, fiebre, abatimiento y anorexia. El síndrome diarreico del cordero aparece en las tres primeras semanas de vida, siendo una de las principales patologías presentes en las granjas.
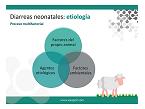
Se trata de un proceso multifactorial que no sólo depende de los agentes infecciosos, sino también de otros factores predisponentes. Cuando uno de estos factores falla, se dan unas determinadas condiciones desfavorables que hacen que la flora digestiva normal del animal comience a proliferar y se desencadene la enfermedad. Por todo ello, en el síndrome diarreico es fundamental conocer cada uno de los factores predisponentes (factores dependientes del animal, factores ambientales y agentes etiológicos) para poder implantar las mejores medidas de prevención.
En España, los agentes más frecuentes que encontramos dentro de los cuadros diarreicos que afectan a animales recién nacidos o lactantes son: Escherichia coli, Clostridium perfringens, Rotavirus y Cryptosporidium spp. Otros agentes como Salmonella sp., Yersinia sp., Campylobacter jejuni y/o Giardia sp. pueden causar, en situaciones muy concretas, un cuadro diarreico.
DIAGNÓSTICO LABORATORIAL
La importancia de un buen diagnóstico, preciso y completo, puede ser vital en muchos aspectos ya que nos permite instaurar las medidas correctoras más idóneas en cada caso.
- TOMA DE MUESTRAS
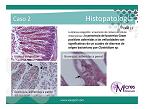
Las mejores muestras son paquetes intestinales completos correctamente anudados para evitar que se derrame el contenido. De esta manera se podrán elegir aquellas zonas que presentan lesiones e incluso utilizar diferentes tramos en función del agente que se esté buscando. Además, al tratarse de tejido, se puede fijar la muestra en formol en el caso de necesitar realizar histopatología. Los hisopos rectales con medio de transporte y las heces son también válidos. No se recomienda enviar el animal entero.
Es importante hacer una buena selección de los animales que se van a muestrear siendo necesario tomar muestras de aquellos con clínica característica, no tratados (ya que esto podría influir a la hora del cultivo microbiológico) y que hayan sido sacrificados o muertos recientemente. Siempre es mejor muestrear varios animales.
Debemos recordar que la interpretación de los resultados obtenidos en el laboratorio depende de la calidad de las muestras recibidas, siendo el manejo previo a su recepción en el laboratorio, crítico para la exactitud de los resultados. Esto se debe a que los microorganismos pueden crecer, multiplicarse o morir rápidamente cuando existe una indebida recolección, transporte y conservación de la muestra.
- ENVÍO DE MUESTRAS
Tras la recogida de las muestras, éstas deben ser enviadas inmediatamente al laboratorio en las siguientes 24 horas, en refrigeración. Solamente se recomienda enviar las muestras congeladas cuando el diagnóstico solicitado se basa exclusivamente en la detección del patógeno mediante la técnica de la PCR. Las muestras deben estar perfectamente identificadas y acompañadas de un informe.
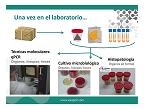
- MÉTODOS LABORATORIALES
Una vez en el laboratorio en primer lugar se realiza una descripción macroscópica de las lesiones observadas y posteriormente se seleccionan las muestras más idóneas para realizar un método u otro.
El cultivo microbiológico de la muestra constituye una técnica básica para poder aislar y posteriormente identificar los microorganismos presentes, a través de la siembra e incubación en medios de cultivo artificiales.
Nos permite obtener las cepas de los agentes patógenos presentes, como Escherichia coli, Salmonella sp. y Clostridium perfringens, así como otras bacterias de menor interés que pueden aparecer en los trastornos digestivos de pequeños rumiantes. Las muestras se siembran en medios de cultivo específicos, se incuban 24-48 horas a 37 grados en condiciones aerobias y anaerobias y de esta forma conseguimos aislar cepas que posteriormente se identifican a través de diferentes metodologías.
Gracias al cultivo microbiológico que nos permite obtener las cepas de los agentes patógenos, podemos identificar aquellos antibióticos a los que una bacteria es sensible o resistente realizando un antibiograma o test de sensibilidad a antibióticos. Para una mayor precisión en el tratamiento es posible realizar la CMI (Concentración Mínima Inhibitoria) que proporciona la concentración o cantidad más pequeña de antibiótico que inhibe o impide la multiplicación bacteriana.
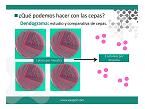
En el caso de Escherichia coli, puede hacerse además una comparación fenotípica de los aislamientos que encontramos. De este modo se obtiene un dendograma que nos ayudará a saber qué cepas están presentes en la explotación, cuales son las más prevalentes etc. Una vez localizadas las distintas cepas, es posible identificar factores de virulencia para clasificarlas como patógenas y realizar un antibiograma en cada una de ellas.
La observación al microscopio puede realizarse sobre la muestra en fresco para ver parásitos u obteniendo un frotis fijado y coloreado mediante distintas tinciones que nos informa sobre la cantidad y morfología bacteriana, además de la presencia de determinados tipos celulares presentes en el preparado. La observación directa de la muestra entrega una información rápida a través de la examinación microscópica de la misma.
Otra técnica muy utilizada es la inmunocromatografía la cual permite detectar el agente etiológico en la muestra en pocos minutos. Son los llamados test rápidos y se basan en la detección de antígenos. Pueden utilizarse a nivel de campo.
Los métodos basados en la detección de ácidos nucleicos como la PCR han tenido un gran avance en los últimos tiempos. Mediante estas técnicas se puede identificar la presencia de numerosos agentes patógenos, incluidos aquellos que no se pueden cultivar, como los virus o los parásitos. Aun cuando se trata de bacterias cultivables, la PCR puede detectarlas en muestras donde la cantidad es muy pequeña, están contaminadas con otras bacterias o muertas. Hoy en día, la PCR a tiempo real (qPCR), es una técnica molecular disponible en los laboratorios que nos permite analizar con gran fiabilidad y rapidez todos los agentes causantes de diarreas en corderos: Rotavirus tipo A, Clostridium perfringens, Cryptosporidium parvum y E. coli. Sin embargo, esta detección no nos permite obtener la cepa ni hacer un antibiograma.
Además de detectar los agentes, con la qPCR podemos identificar ciertas características de algunas bacterias que nos permite clasificarlas más allá del nivel de especie. Se aplica fundamentalmente para la detección de factores de virulencia de E. coli y para las toxinas de C. perfringens.
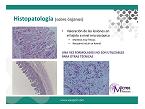
Por último la histopatología estudia las lesiones microscópicas de los tejidos. Cuando en una analítica se detectan varios agentes patógenos, el estudio histopatológico nos ayudará a valorar cual es el agente primario de las lesiones y de esta manera orientar el tratamiento y prevención.
En resumen, para realizar un buen diagnóstico diferencial de diarreas en corderos lactantes, el diagnóstico laboratorial es una herramienta que nos va a servir para detectar los patógenos específicos con aquellas técnicas que nos permitan identificarlos. Un diagnóstico completo y preciso deberá incluir:
* Cultivo microbiológico y antibiograma.
* Detección de Rotavirus, Cryptosporidium y Clostridium perfringens (qPCR).
* Detección de factores de virulencia de E. coli mediante qPCR y/o realización de dendograma.
* Realización de toxinotipado de Cl. perfringens si muestra positiva (qPCR).
* Histología.
Oviespaña, noticias diarias sobre el mercado nacional e internacional del ovino, investigación ganadera, alimentación y sistemas de manejo.